EQUIPE RITM
Radiopharmaceutiques, Imagerie, Théranostiques et Multimodalité
Contexte scientifique et enjeux
L’équipe RITM développe et évalue des médicaments radiopharmaceutiques originaux, essentiellement basés sur des radioisotopes métalliques. Ces composés sont conçus dans le cadre d’une approche théranostique et visent à améliorer le diagnostic précoce des patients et leur prise en charge thérapeutique.
Dans ce but, l’équipe RITM développe de nouveaux outils moléculaires et méthodologies permettant l’optimisation des différents éléments constitutifs d’un radiopharmaceutique (vecteur, chélateur, espaceur, lien de bioconjugaison, etc.) et leur évaluation in vitro et in vivo. Les compétences des membres de RITM s’étendent de la chimie de coordination à la chimie des peptides, de la bioconjugaison à la radiochimie, de la radiopharmacie à l’imagerie nucléaire préclinique.
Membres de l’équipe

Responsable : Dr. Victor GONCALVES (MCF)
- Dr. Bertrand COLLIN (PU-PH)
- Pr. Franck DENAT (PR)
- Dr. Sophie POTY (CPJ, UBE)
- Dr. Ibai VALVERDE (CR CNRS)
- Dr. Michael CLARON (IE CNRS)
- Cécile DESINGLE (Tech UBE)
- Dr. Mathieu MOREAU (IE UBE)
Axes de recherche
Axe 1 : Outils moléculaires pour la conception de nouveaux radiopharmaceutiques

En savoir plus sur nos 3 thématiques de recherche :
Agent chélatant et radiochimie
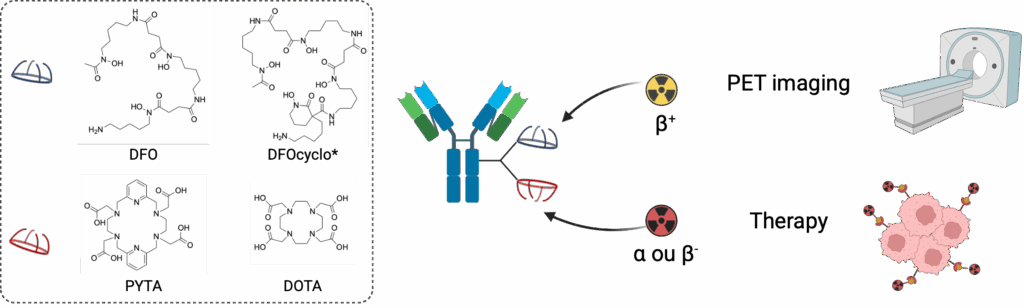
L’agent chélatant bifonctionnel est un élément clé dans le design de radiopharmaceutiques. Introduit sur une molécule vectrice, il assure la coordination stable, in vivo, de radioisotopes métalliques. L’équipe possède une expertise reconnue internationalement dans le domaine, qui s’est traduit notamment par la création de la spin-off CheMatech. Ces recherches se poursuivent avec le développement de nouveaux agents chélatants bifonctionnels aux propriétés optimisées. Ces travaux se focalisent en particulier sur des agents chélatants capables de former, à température ambiante, des complexes thermodynamiquement stables et cinétiquement inertes avec des « couples théranostiques » tels que 89Zr/177Lu, 89Zr/225Ac ou 64Cu/67Cu. Dans cette approche, le radiotraceur sert de « compagnon diagnostique » de l’analogue thérapeutique. Une autre part de nos activités de recherche est tournée vers le design d’agents chélatants de radiométaux émetteurs a qui connaissent un intérêt grandissant pour la radiotherapie interne vectorisée (RIV), tels que 225Ac, 212Pb, 227Th, 223Ra et le développement des méthodes de radiochimie associées.
Solutions de bioconjugaison
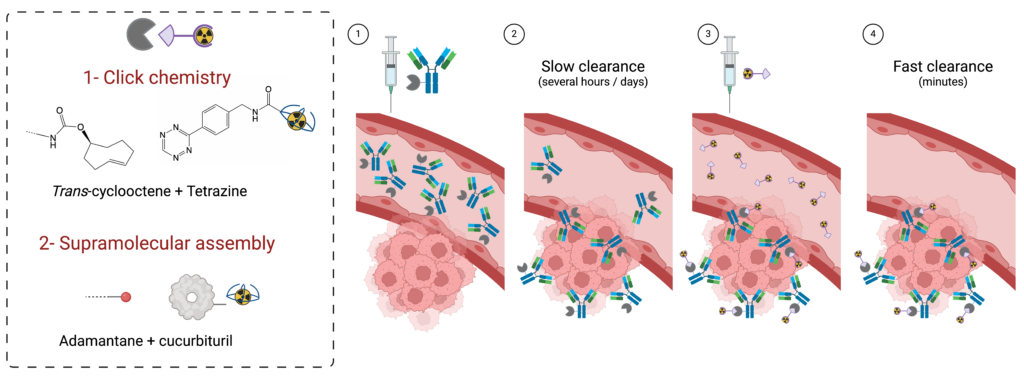
L’étape de greffage d’un agent chélatant à un biovecteur est appelée bioconjugaison. Elle joue un rôle critique dans le design de radiopharmaceutiques. La chimie mise en jeu doit obéir à un nombre important de contraintes, notamment lorsqu’elle est mise en œuvre sur des biomolécules complexes et fragiles telles que les protéines. L’équipe a développé une expertise dans la modification chimique d’une grande variété de vecteurs, tels que les anticorps, leurs fragments, les peptides ou encore les petites molécules. Les techniques mises en jeu permettent des greffages dits « site-spécifiques », permettant un contrôle précis du nombre et de la position des modifications effectuées. Ce savoir-faire est mis à disposition de la communauté via la Transfer unit Bioconjugates. Nos travaux en cours portent sur le développement de plateformes permettant le marquage multiple de protéines sur un seul résidu, et d’outils destinés aux approches de pré-ciblage mettant en jeu la chimie click ou la chimie supramoléculaire.
Vectorisation et ciblage moléculaire
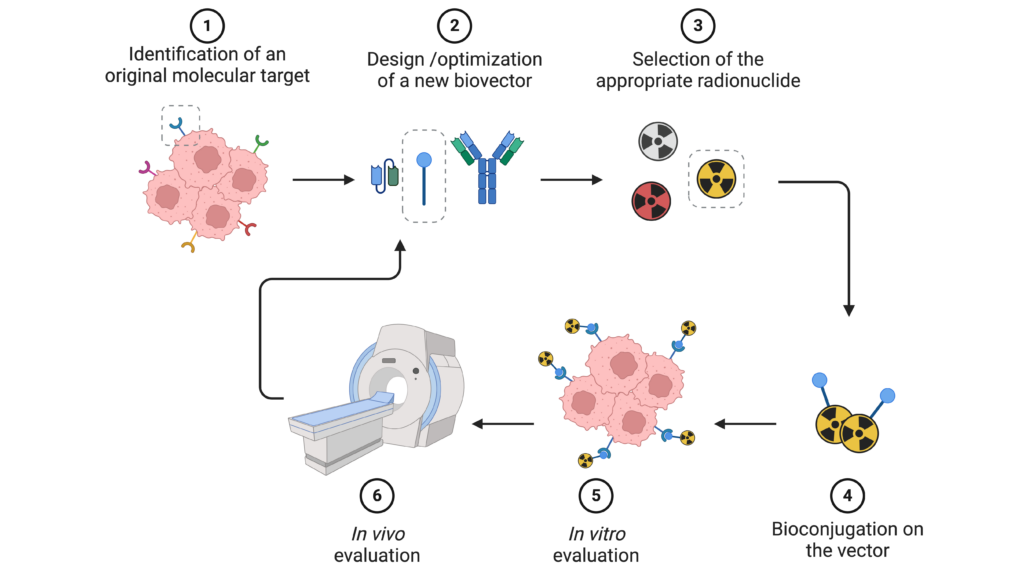
Par-delà les vecteurs classiques (trastuzumab, pertuzumab, PSMA, FAPI, …), qui nous servent à la validation de nouveaux outils moléculaires et méthodologies, l’équipe s’intéresse également à la validation de nouvelles cibles pharmacologiques et au développement de nouveaux vecteurs de ciblage. L’objectif est d’identifier des cibles moléculaires permettant de répondre à des besoins cliniques non satisfaits à ce jour. Ces travaux s’inscrivent dans les domaines de :
– l’oncologie (ciblage du stroma tumoral, de l’hypoxie, etc. ) en particulier pour des cancers à mauvais pronostic tels que les cancers du pancréas et le glioblastome
– imagerie de la fibrose, dans pathologies telles que la fibrose pulmonaire idiopathique,
– l’imagerie de l’arthérosclérose.
Les compétences disponibles en interne permettent la synthèse et l’ingénierie d’une très grande variété de vecteurs, allant des petites molécules hétérocycliques, jusqu’à des anticorps entiers ou des aptamères oligonucléotidiques. L’optimisation de ces vecteurs passe également par des approches multi (hétéro)valentes, dans lesquelles plusieurs vecteurs sont combinés dans un composé unique afin d’augmenter l’affinité et/ou la sélectivité des radiopharmaceutiques.
Exemples de publications de l’axe 1
- Moving beyond isothiocyanates: A look at the stability of conjugation links towards radiolysis in 89Zr-labeled immunoconjugates. R. Vizier, P. Adumeau, M. Moreau, V. Goncalves, F. Denat.
Bioconjugate Chemistry (2024), 35, 633–637 - Synthesis and Preclinical Fluorescence Imaging of Dually Functionalized Antibody Conjugates Targeting Endothelin Receptor-Positive Tumors, D. Vivier, M. Hautière, D. Pineau, PA. Dancer, A. Herbet, JP. Hugnot, C. Bernhard, V. Goncalves, C. Truillet, D. Boquet, F. Denat.
Bioconjugate Chemistry (2023), 34, 2144-2153 - SPECT Imaging of Lysyl Oxidase-like 2 in a Model of Idiopathic Pulmonary Fibrosis, R. Vizier, AR. Garnier, A. Dias, M. Moreau, M. Claron, B. Collin, F. Denat, PS. Bellaye, V. Goncalves.
Molecular Pharmaceutics (2023), 20, 3613-3622.
Axe 2 : Approche radiothéranostique et multimodalité
En savoir plus sur nos 3 thématiques de recherche :
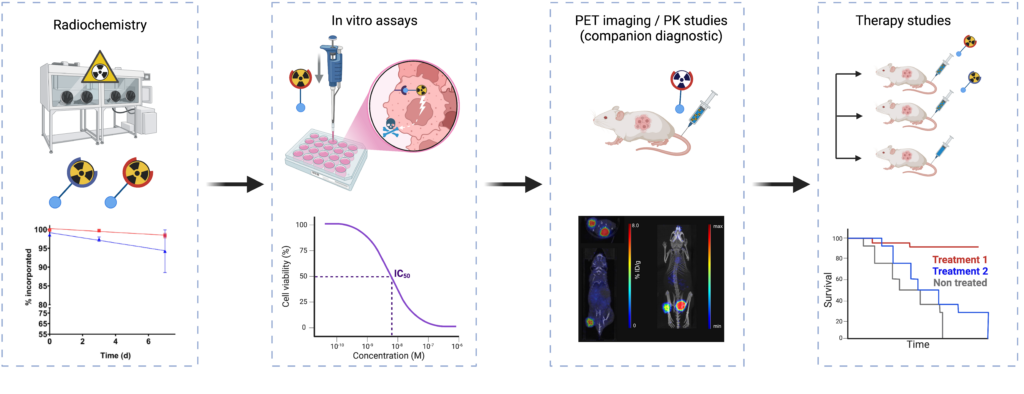
Radiothérapie interne vectorisée et radiothéranostiques
La radiothérapie interne vectorisée (RIV) occupe une place croissante dans l’arsenal thérapeutique en oncologie. Cette stratégie permet une irradiation systémique très sélective des tumeurs cancéreuses, quels que soient leur nombre et leur localisation. Elle repose sur l’emploi d’un radiopharmaceutique vectorisé, spécifique d’une cible tumorale, véhiculant un radioisotope dont les particules émises (particules β-, α- ou électrons Auger) sont capables d’induire la mort des cellules cancéreuses. Notre ambition est de nous positionner sur cette thématique résolument interdisciplinaire et translationnelle, grâce à notre maîtrise des divers maillons de la chaîne de développement de composés radiopharmaceutiques pour la RIV, depuis la chimie jusqu’aux essais cliniques. Ces projets, par nature collaboratifs, sont menés au sein de consortiums impliquant des partenaires académiques, hospitaliers, et souvent industriels. Nos programmes portent notamment sur le développement de nouvelles molécules pour la RIV pour les patients atteints de cancer colorectal métastatique (projet COMETE) et l’étude de la combinaison de la RIV à d’autres modalités thérapeutiques (projet 2in1 ADRC).
TEP/IRM
L’imagerie simultanée par tomographie par émission de positons (TEP) et résonance magnétique (IRM) combine deux modalités complémentaires, offrant des informations fonctionnelles et moléculaires (TEP) et anatomiques et métaboliques (IRM).
Cette synergie a transformé l’imagerie biomédicale, tant en recherche préclinique qu’en pratique clinique, grâce à ses capacités d’intégration unique. Dans ce contexte, nous avons obtenu sur la période 2012-2024, le projet EQUIPEX (PIA 1) IMAPPI (Integrated Magnetic resonance And Positron emission tomography in Preclinical Imaging – ANR-10-EQPX-0005, 7,3 M€). L’objectif d’IMAPPI a été le développement d’un instrument d’imagerie TEP (détecteurs solides SiPM)-IRM(7 T) simultanée, système commercial depuis 2017 .
Cette technologie représente une avancée majeure recherche en translationnelle / transversale, particulièrement en oncologie, cardiologie, développement instrumental et chimie des agents diagnostiques. En oncologie, elle combine la sensibilité moléculaire de la TEP, permettant de détecter l’activité métabolique et les récepteurs spécifiques, avec la précision anatomique et fonctionnelle de l’IRM pour localiser et caractériser les tumeurs et métastases, notamment dans les tissus mous complexes. En cardiologie, elle intègre l’évaluation métabolique myocardique (TEP) avec des analyses structurelles et de perfusion détaillées (IRM), optimisant ainsi le diagnostic des cardiopathies. Du point de vue instrumental, l’intégration de ces deux modalités nécessite des technologies avancées pour gérer les interférences magnétiques et optimiser les acquisitions simultanées au profit des pathologies que nous étudions. Enfin, en chimie, le développement d’agents de contraste paramagnétiques et de radiopharmaceutiques spécifiques permet d’améliorer la spécificité et la sensibilité vis-à vis des biomarqueurs ciblés, ouvrant la voie à des applications en médecine personnalisée et à l’exploration de nouvelles cibles thérapeutiques.
Cette synergie multidimensionnelle place la TEP-IRM au cœur des innovations diagnostiques modernes dans lesquelles notre groupe est particulièrement actif.
Multimodalité : couplage de l’imagerie nucléaire et l’imagerie optique
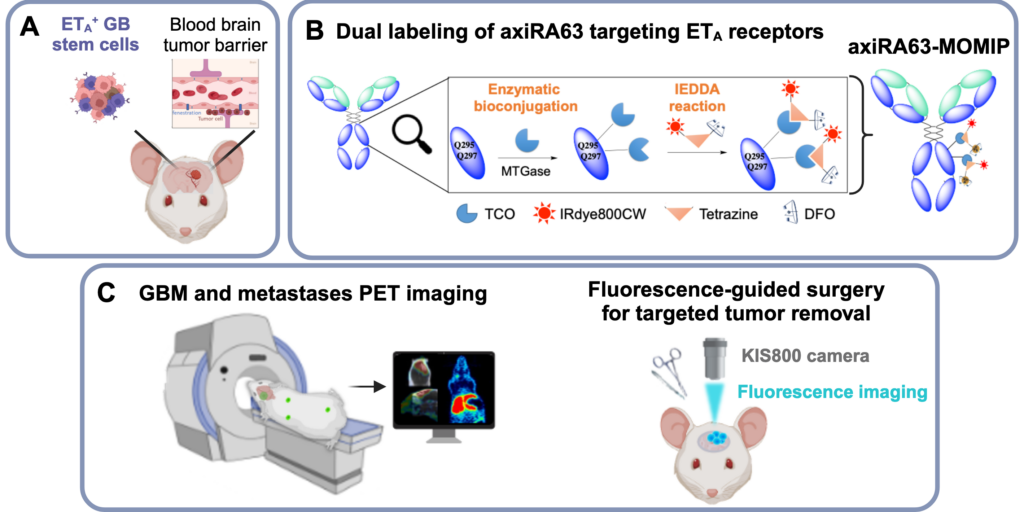
De façon analogue à l’imagerie TEP/IRM, la bimodalité nucléaire/optique vise à combiner les avantages de ces deux techniques, au sein d’une molécule unique, afin d’améliorer le diagnostic précoce et la prise en charge thérapeutique des patients. L’imagerie nucléaire (TEP ou SPECT) permet la détection des tumeurs, et éventuelles métastases, et la stratification des patients. L’imagerie de fluorescence, peu pénétrante, mais non ionisante, améliore quant à elle intérêt la résection des tumeurs en permettant au chirurgien de distinguer visuellement les tissus sains des tissus pathologiques. L’équipe conçoit des sondes vectorisées combinant les deux modalités, qui sont évaluées dans des modèles précliniques de cancers à mauvais pronostic tels que le glioblastome et le cancer du pancréas.
Exemples de publications de l’axe 2
- Preoperative PET imaging and fluorescence-guided surgery of human glioblastoma using dual-labeled antibody targeting ETA receptors in a preclinical mouse model: A theranostic approach. M. Hautiere, D. Vivier, P. Dorval, D. Pineau, D. Kereselidze, C. Denis, A. Herbet, N. Costa, C. Bernhard, V. Goncalves, E. Selingue, B. Larrat, P.-A. Dancer, J.-P. Hugnot, D. Boquet, C. Truillet, F. Denat. Theranostics (2024), 14, 6268-6280
- SPECT Imaging of Lysyl Oxidase-like 2 in a Model of Idiopathic Pulmonary Fibrosis. R. Vizier, AR. Garnier, A. Dias, M. Moreau, M. Claron, B. Collin, F. Denat, PS. Bellaye, V. Goncalves.
Molecular Pharmaceutics (2023), 20, 3613-3622. - Modular One-Pot Strategy for the Synthesis of Heterobivalent Tracers. T. Bailly, S. Bodin, V. Goncalves, F. Denat, C. Morgat, A. Prignon, IE Valverde.
ACS Medicinal Chemistry Letters (2023), 14, 636-644
Projets en cours
Nous bénéficions du soutien de divers agences et dispositifs régionaux (FEDER, Graduate Program INTHERAPI, Cancéropole Est), nationaux (ANR, INCA, FLI Imaging) et internationaux (Horizon Europe). Une part de nos recherches sont également menées en partenariat avec des entreprises biotech du domaine des radiopharmaceutiques (Oncodesign Precision Medicine, Radiomune Pharma).